I løpet av livet vil mange utvikle kreft; Imidlertid har dødeligheten generelt gått ned over tid, hovedsakelig på grunn av forbedrede behandlingstilbud. Immunkontrollpunkthemmere er en av de mest moderne kreftbehandlingsalternativene. Disse stoffene øker overlevelsen i de fleste kreftformer. De forventes å bli brukt mer og mer og for flere indikasjoner [1].
Flere immunkontrollpunkthemmere er identifisert, inkludert CTLA-4 (cytotoksisk T-lymfocyttantigen 4), PD-1 (programmert celledødsreseptor 1) og PD-L1 (liganden for PD-1) [2].
PD-1-reseptoren uttrykkes på overflaten av aktive T-celler og når PD-1 binder seg til PD-L1, genereres et hemmende signal som regulerer T-celleaktiviteten og demper immunresponsen. Ved å hemme PD-1 kan man da gjenopprette funksjon og derved behandle svulster som selv uttrykker PD-L1 og utløser celledød. Som en bivirkning kan imidlertid selvreaktive T-celler overleve og forårsake cytotoksiske bivirkninger [2]. Noen vanlige bivirkninger består derfor av hudutslett av forskjellig art, kløe, lungebetennelse eller kolitt med blant annet abscesser i den nøytrofile krypten og apoptose av epitelceller [3, 4]. Noen studier har vist bedre behandlingsrespons hvis pasienter opplever mildere immunrelaterte bivirkninger som hudutslett.
Pasienter kan også lide av endokrinologiske bivirkninger [5]; blant annet er hypofysitt, tyreoiditt og type 1 diabetes observert [4, 6, 7]. Å utvikle diabetes som krever rask innsettende insulin er en sjelden, men kjent bivirkning. Forekomsten av dette har blitt notert å være omtrent 1 %. [8].
Det ser også ut til å være en sammenheng mellom PD-1 og diabetes selv uten behandling, ettersom en studie fant redusert PD-1-ekspresjon i T-celler hos personer med type 1-diabetes sammenlignet med friske individer [9].
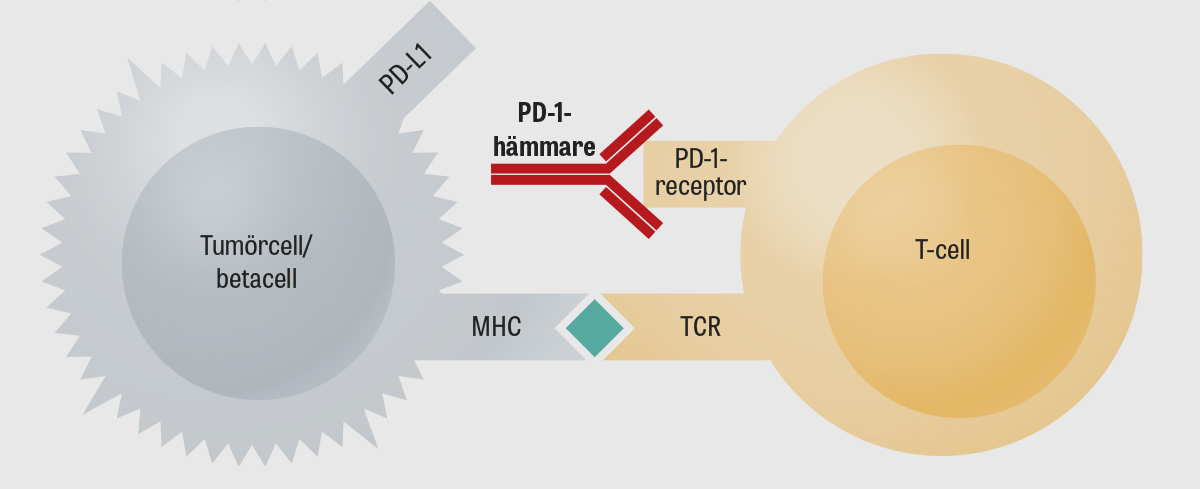
Betaceller i bukspyttkjertelen uttrykker PD-L1, og når PD-1-hemmerbehandling settes i gang, svikter PD-1-PD-L1-signalering og hemming av autoreaktive T-celler forekommer ikke. De selvreaktive T-cellene kan da ødelegge betacellene og forårsake insulinkrevende diabetes [4, 7] (Figur 1). Insulinkrevende diabetes ser også ut til å være mer vanlig når den behandles med PD-1-hemmere enn med anti-CTLA-4 immunkontrollpunkthemmere [10]. Insulinkrevende diabetes er en sjelden bivirkning, med tidligere studier som viser en forekomst på 0,6-1,9 % [7, 11].
Nivolumab er en slik immunkontrollpunkthemmer. Det er et IgG4 monoklonalt antistoff som binder seg til PD-1-reseptoren og hemmer dens effekt. Dette fører til en forbedret T-cellerespons og gir en antitumoreffekt. Nivolumab er for tiden indisert for behandling av avansert melanom hos voksne. Det er også indikasjoner for blant annet ikke-småcellet lungekreft, pleural mesothelioma, Hodgkins lymfom og enkelte gastrointestinale maligniteter. Studier har vist god effekt på malignt melanom, hvor det er observert økt residivfri overlevelse [12, 13].
Vi beskriver et tilfelle der en pasient med metastatisk malignt melanom fikk diabetesrelatert ketoacidose kort tid etter behandling med nivolumab.
Saksbeskrivelse
En 72 år gammel mann med hypertensjon, kontinuerlig positivt luftveistrykk (CPAP)-behandlet obstruktivt søvnapnésyndrom og metastatisk malignt melanom med pågående immunterapi ankom akuttmottaket med ambulanse på grunn av kvalme og nedsatt allmenntilstand. Før den akutte sykdommen var pasienten i god form, vital og aktiv. Pasienten hadde stabile vitale tegn med metning på 98 % i luft, respirasjonsfrekvens 20/min, blodtrykk 112/64 mm Hg, puls 97/min og temperatur 35,7°C. I staten ble pasienten registrert å ha sløret tale og var sliten og opptatt, men tilstrekkelig og fullt orientert. For laboratorieresultater, se tabell 1.
Pasienten ble alvorlig syk av diabetes, uttalt ketoacidose og sekundær akutt nyresvikt. Pasienten ble behandlet i henhold til den lokale behandlingsplanen for diabetisk ketoacidose. Etter 32 timers insulininfusjonsbehandling forsvant acidosen og pasienten fikk insulin i et 4-doseregime. Kreatininnivået normaliserte seg gradvis i løpet av behandlingsperioden. Prøvetaking viste negative GAD- og IA2-antistoffer. HbA1c ved gjenbesøket var det 65 mmol/mol. Dessverre ble ikke C-peptid tatt i behandlingsperioden.
Pasienten hadde fått den åttende dosen nivolumab, en PD-1-hemmer, 11 dager tidligere. Tidligere blodsukkerverdier ved månedlige kontroller hadde vært normale. Pasienten hadde blitt raskt syk, hadde ingen kjent arvelighet for diabetes og hadde negative autoantistoffer. Samlet sett ble dette vurdert som utbruddet av diabetes med nivolumab-indusert ketoacidose i fravær av andre mer plausible forklaringer.
Ett år etter at han ble syk, trenger pasienten fortsatt insulin. Nivolumab ble seponert i forbindelse med ketoacidose. Behandlingsregimet ble endret til en kombinasjon av BRAF- og MEK-hemmere (dabrafenib og trametinib), medikamenter som blokkerer en kinase som bidrar til å drive tumorutvikling ved malignt melanom med en BRAF-mutasjon.
Diskusjon
Endokrine bivirkninger er ikke uvanlige ved behandling med immunsjekkpunkthemmere. Diabetes er en kjent, men sjelden bivirkning. Sykdommen oppstår ofte akutt, noe som støttes av det lave nivået av C-peptid og HbA1c1c ofte moderat lav ved debut [4]. Autoantistoffer forekommer hos omtrent 50 % av pasientene som utvikler diabetes når de behandles med immunkontrollpunkthemmere, sammenlignet med 85 % av pasientene med vanlig type 1 diabetes [4, 8]. Pasienter som er positive for GAD-antistoffer ser imidlertid ut til å ha en tendens til å utvikle diabetes før PD-1-hemmerbehandling sammenlignet med de som er negative [8, 14]. Selv om flertallet (76%) har ketoacidose, har de antistoffpositive en økt risiko for ketoacidose i tillegg til tidlig debut [8].
Med tanke på alvorlighetsgraden av akutt innsettende diabetes, er det anbefalinger om å overvåke blodsukkeret før legemiddeladministrering under pågående behandling med immunkontrollpunkthemmere [15, 16]. Diabetes indusert av behandling med PD-1-hemmere har en tendens til å komme raskt, og noen mener at regelmessig blodsukkermåling ikke er nyttig for å forutsi utbruddet av diabetes [7], noe som også var tilfelle med vår pasient. Andre anbefaler en kombinasjon av pasientopplæring, blodsukkerovervåking og hjemmeblodsukkerovervåking [4].
Immunkontrollpunkthemmer-indusert diabetes oppstår når en stor prosentandel av betacellene er ødelagt og disse pasientene blir permanent insulinavhengige [4, 8]. Det er gjort forsøk med høydose kortison for å behandle bivirkningen, men uten hell [17].
Konklusjon
Immunsjekkpunkthemmere er relativt nye preparater som i økende grad brukes klinisk. Å utvikle diabetes med ketoacidose er en sjelden, men alvorlig bivirkning av PD-1-hemmere. Det var ikke mulig å forutsi når pasienten under den pågående behandlingen kan bli påvirket. Sykdommen er ofte akutt og ca 75 % utvikler ketoacidose, hvorav ca 50 % har lavt C-peptid og kun en tredjedel er antistoffpositive [18]. Fordi sykdommen i stor grad er akutt, er det viktig at pasientene informeres slik at de kan gjenkjenne symptomer og oppsøke akutthjelp ved behov. Bevissthet hos omsorgspersoner er også viktig på grunn av det økende antallet pasienter som behandles med PD-1-hemmere.
Potensielle hookups eller sjalu forhold: Ingen oppgitt.
Medisinsk journal. 2023;120:23039
Medisinsk tidsskrift 27-31/2021
Lakartidningen.se

«Lidenskapelig spiller. Venn av dyr overalt. Generell alkoholevangelist. Banebryter for sosiale medier. Zombie-nerd.»